CuS có tác dụng với H2SO4 loãng không? Cùng tìm hiểu nhé
CuS có tác dụng với H2SO4 loãng không? Còn H2SO4 đặc nóng thì sao? Chất này tác dụng được với những acid nào?
Nếu như bạn có những thắc mắc đó thì hãy đọc ngay bài viết này nhé. Đọc để bạn có thể biết được rằng đặc điểm của một số muối sunfua, trong đó có CuS nhé. Đọc để có thể ôn tập những kiến thức hóa học này nhé bạn. Để bạn biết được rằng CuS có tác dụng với H2SO4 loãng không.

CuS có tác dụng với H2SO4 loãng không
Content
Đặc điểm của muối sunfua
Các muối tan trong nước: Muối ѕunfua của các kim loại nhóm IA, IIA (trừ Be) như Na2S, K2S,… khi tác dụng với HCl, H2SO4 loãng sẽ sinh ra khí H2S.
Các muối không tan trong nước nhưng tác dụng với HCl, H2SO4 loãng sinh ra khí H2S như ZnS, FeS,…
Các muối không tan trong nước, không tác dụng với HCl, H2SO4 nhưng lại tác dụng với H2SO4 đặc nóng, HNO3 đặc nóng như: CuS, FeS2, PbS, Ag2S, HgS, CuFeS2,..
Màu sắc của một số muối sunfua như sau: ZnS: Trắng; FeS, PbS, CuS: Đen; CdS: Vàng; HgS: Đỏ.
CuS có tác dụng với H2SO4 loãng không
Bạn có biết câu trả lời cho câu hỏi CuS có tác dụng với H2SO4 loãng không thì trước tiên hãy thử tìm hiểu về tính chất hóa học của hai chất này nhé. Xem rằng hai chất này là gì? Liệu rằng có khả năng tác dụng với nhau để mà tạo thành một chất mới hay không? Liệu rằng một phương trình hóa học có thể xảy ra giữa hai chất này hay không nhé.
Đặc điểm của CuS

Đây là một hợp chất hóa học của đồng và lưu huỳnh có tên gọi là đồng(II) sulfide, hay đồng monosulfide. Hợp chất này trong tự nhiên có màu đen chàm xanh. Và tủa CuS màu đen sẽ được tạo thành khi ta sục khí H2S qua dung dịch muối Cu(II)
Để trả lời cho câu hỏi CuS có tác dụng với H2SO4 loãng không hay không thì như phần trên ta đã có câu trả lời là không rồi, CuS sẽ tác dụng với H2SO4 đặc nóng theo phương trình sau:
CuS+4H2SO4(đậm đặc, nóng)=CuSO4+4SO2↑+4H2O
Đặc điểm của H2SO4
Acid sulfuric, còn được gọi là vitriol, là một acid vô cơ gồm các nguyên tố lưu huỳnh, oxy và hydro, có công thức phân tử H2SO4. Nó là một chất lỏng không màu, không mùi và sánh, hòa tan trong nước, trong một phản ứng tỏa nhiệt cao.
Chất này có tính ăn mòn mạnh, ngoài ra còn có tính chất khử nước và oxy hóa. Dễ hút ẩm, dễ dàng hấp thụ hơi nước từ không khí. Khi tiếp xúc, acid sulfuric có thể gây bỏng hóa chất nghiêm trọng và thậm chí bỏng nhiệt thứ cấp; chất này rất nguy hiểm ngay cả ở nồng độ vừa phải.
Acid sulfuric là một hóa chất công nghiệp rất quan trọng, và sản lượng acid sulfuric của một quốc gia là một chỉ số tốt về sức mạnh công nghiệp của quốc gia đó. Nó được sản xuất rộng rãi với các phương pháp khác nhau, như quy trình tiếp xúc , quy trình acid sulfuric ướt, quy trình buồng chì và một số phương pháp khác.
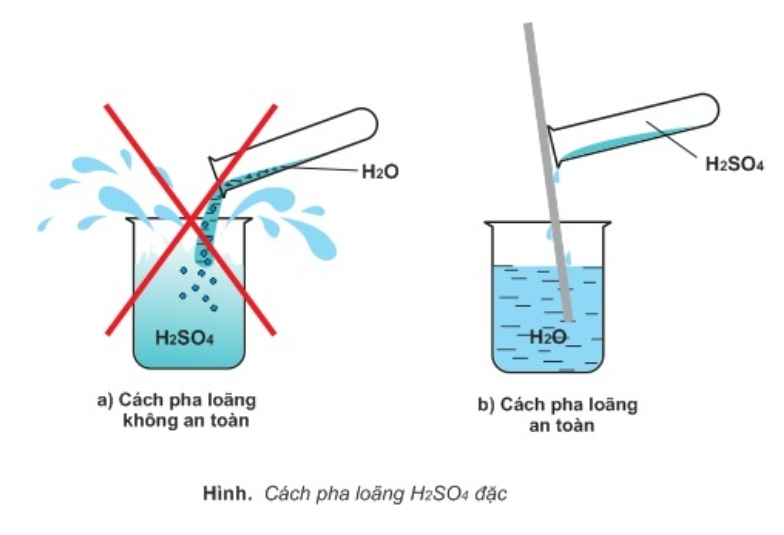
Tại sao CuS không tác dụng với H2SO4 loãng
Nguyên nhân mà CuS không tác dụng với H2SO4 loãng là bởi acid này có nồng độ loãng, không đủ để có thể xảy ra phản ứng oxy hóa khử như khi CuS tác dụng với dung dịch H2SO4 đặc nóng.
CuS có tác dụng với H2SO4 đặc nóng không
Nhờ vào phần đặc điểm, tính chất của muối sunfua mà ta biết rằng CuS có tác dụng với dung dịch H2SO4 đặc nóng theo phương trình hóa học sau:
CuS+4H2SO4(đậm đặc, nóng)=CuSO4+4SO2↑+4H2O
FeS có tác dụng với H2SO4 loãng không
Nhờ vào phần đặc điểm, tính chất của muối sunfua mà ta biết rằng FeS có tác dụng với dung dịch H2SO4 loãng theo phương trình hóa học sau:
FeS + H2SO4 → FeSO4+ H2S
Mong rằng sau khi biết được CuS có tác dụng với H2SO4 loãng không bạn có thể tiếp tục ôn tập những kiến thức hóa học khác nhé. Hãy luôn cố gắng cũng như nỗ lực thật nhiều để nâng cao kiến thức của bản thân bạn. Bởi một ngày nào đó bạn sẽ nhận ra rằng học hỏi là không bao giờ nhầm lẫn hay sai trái đâu. Vì thế hãy luôn học thật nhiều bạn nhé, học cho chính bản thân bạn của mai này ấy.
- Xem thêm: Thuốc elthon giá bao nhiêu? Dùng để điều trị bệnh gì?
Thuốc elthon giá bao nhiêu? Dùng để điều trị bệnh gì?
Samsung A22 5G giá bao nhiêu? Có phù hợp với bạn không?
Realme Q3 giá bao nhiêu? Có đắt so với giá trị của nó không?
Quần size S là bao nhiêu kg? Mỗi size phù hợp với người nào
4 tuần là bao nhiêu ngày? Cách tính tuổi thai đúng nhất
1 byte bằng bao nhiêu bit? Mối liên hệ giữa 2 đại lượng này?
1 gam bằng bao nhiêu gram? Hai đại lượng này có giống nhau?
